Nature Methods | 光遗传学新突破:控制单分子释放的创新方法
来源:生物探索 2024-03-17 10:15
光敏蛋白的设计通常基于自然界中存在的光感受蛋白。通过基因工程技术,研究人员对这些天然蛋白进行改造,以适应特定的实验需求。
Nature Methods报道了该领域的最新进展“An optogenetic method for the controlled release of single molecules”。

Highlights
该研究开发了一种新的光遗传学(optogenetics)方法,用于在活细胞中控制单分子(single molecule)的释放。研究团队通过结合一种可光解的蛋白质(photocleavable protein)实现了这一目标,这种蛋白质在近紫外光(near-ultraviolet light)照射下会发生裂解,从而释放绑定的目标分子。
这项技术的关键创新之处在于,它可以精确控制细胞内功能性单分子的释放,并允许研究人员在单分子水平上观察和分析蛋白质在活细胞中的行为。通过这种方法,研究人员能够在细胞质和细胞膜上进行单分子成像(single-molecule imaging),大大简化了对任何蛋白质在活细胞中的单分子显微镜(single-molecule microscopy)研究的可及性。
此外,这种技术还展示了通过控制释放的方式重构离子通道导电性(ion channel conductance)和恢复敲除细胞中的信号通路(signaling pathway)的潜力。通过释放一种在敲除细胞中缺失的关键激酶,研究者成功地重建了免疫细胞中的信号转导通路。
这项研究为单分子水平上研究细胞功能提供了一个强大的新工具,并可能对未来的生物学和医学研究产生重要影响。
Strategies
设计和构建光解蛋白复合体(Photocleavable Protein Complex):研究团队首先构建了一个含有光解蛋白PhoCl的复合体。PhoCl是一种在近紫外光(near-ultraviolet light)照射下可以发生裂解的绿红色光转换蛋白(photoconvertible protein)。这种裂解将切断肽链,从而释放与其相连的目标蛋白(target protein)。
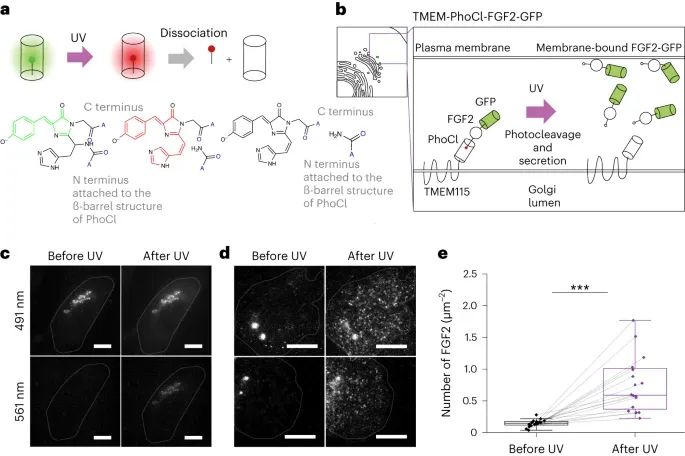
通过 PhoCl 蛋白进行光控制的方法,用来释放细胞中的胞浆蛋白 FGF2-GFP。这一过程通过 PhoCl 蛋白的光解活性来实现,即在近紫外光的激活下,PhoCl 蛋白被光解,导致与其连接的目标蛋白(在这个例子中是 FGF2-GFP)从细胞器(如高尔基体)释放到胞浆中。这个方法允许研究者以光剂量依赖的方式,将功能性蛋白以适合单分子成像的量传递到细胞质和质膜中,从而简化了对活细胞中任何蛋白质的单分子显微镜技术的要求。(Credit: Nature Methods)
融合目标蛋白和锚定蛋白(Protein Fusion and Anchoring):然后,研究者将目标蛋白与PhoCl融合,并进一步与位于高尔基体(Golgi apparatus)的锚定蛋白(anchoring protein)相连接。这样,目标蛋白在未经光解之前被限制在高尔基体。
近紫外线照射(Near-Ultraviolet Illumination):在实验中,研究者通过短暂的近紫外光脉冲照射细胞,触发PhoCl的裂解,导致与其融合的目标蛋白从高尔基体释放到细胞质或细胞膜。
单分子成像(Single-Molecule Imaging):释放的目标蛋白可用于单分子成像研究。研究者利用这种方法,能够在单分子水平上观察和分析蛋白质在活细胞中的行为和功能。
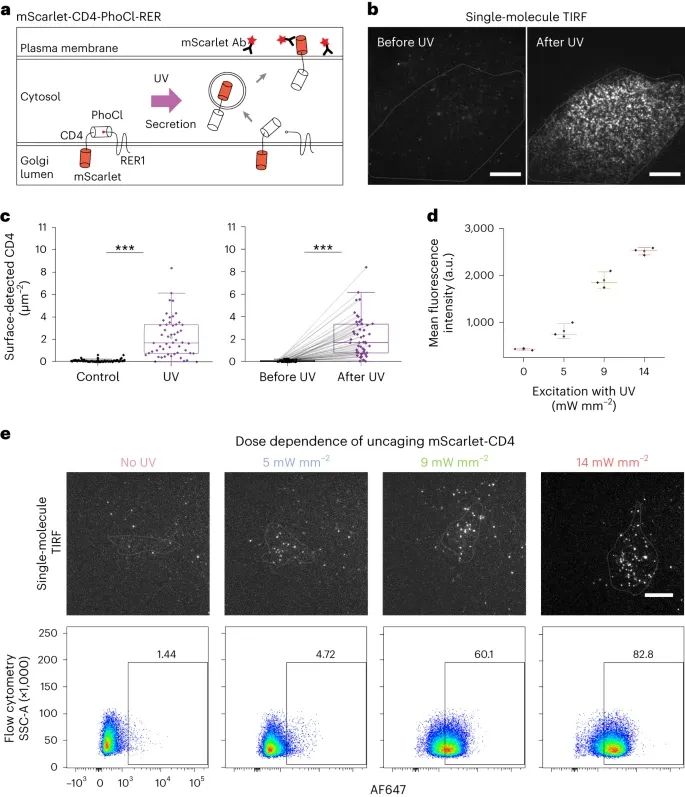
使用 PhoCl 蛋白的光解活性来控制跨膜蛋白 CD4 的释放。研究人员构建了一个含有 mScarlet-CD4、PhoCl 和 Golgi-定位蛋白 RER 的融合构建物。这个构建物被锚定在高尔基体上。在紫外光照射下,PhoCl 蛋白发生光解,导致与其连接的 CD4 蛋白从高尔基体释放,并被运输到细胞膜上。通过使用 TIRF 显微镜技术,可以观察到单分子层面上 mScarlet-CD4 的动态。这个过程展示了如何利用 PhoCl 蛋白实现对跨膜蛋白功能和定位的光学控制,从而促进对细胞膜蛋白功能的单分子研究。(Credit: Nature Methods)
功能性研究(Functional Studies):除了观察蛋白质的行为,研究者还利用这一技术研究了蛋白质的功能,如离子通道导电性(ion channel conductance)的重建和信号通路(signaling pathways)的恢复。
Behind the Scenes
光遗传学释放单分子的工作原理
光敏蛋白的设计和原理
光遗传学技术的核心在于光敏蛋白的设计和应用,这些特殊的蛋白质能够响应特定波长的光照而发生结构上的改变,从而实现对细胞内过程的精确控制。光敏蛋白的设计灵感多源自自然界中的光感受器,如绿藻中的ChR2(通道蓝藻蛋白-2),其能够在蓝光照射下开启离子通道,控制细胞内的电位变化。
光敏蛋白的种类
光敏蛋白大致可以分为两类:一类是作为离子通道或泵,在光照下直接影响细胞的膜电位和内部离子浓度;另一类则通过光诱导的结构变化,激活或抑制特定的生物分子,进而影响细胞内的信号传递路径。这两种机制各有优势,选择哪一种取决于研究目的和对象。
设计原理
光敏蛋白的设计通常基于自然界中存在的光感受蛋白。通过基因工程技术,研究人员对这些天然蛋白进行改造,以适应特定的实验需求。例如,通过改变光敏蛋白的氨基酸序列,可以调整其对光的敏感波长,从而实现对光信号的精确控制。
光敏蛋白的设计要考虑多个因素,包括光敏蛋白对光的敏感度、激活和关闭的速度、以及是否易于被细胞表达和容纳。此外,为了实现更精细的控制,研究人员还在不断开发新的光敏蛋白变体,以适应不同波长的光照和不同类型的细胞。
在实际应用中,光敏蛋白通常通过遗传工程的方式引入目标细胞,与特定的生物分子融合,形成一个能够响应光照的融合蛋白。当受到特定波长的光照射时,融合蛋白发生构象变化,激活或释放与之结合的生物分子,从而实现对细胞功能的调控。
短脉冲光源的作用机制
在光遗传学领域,短脉冲光源的应用是实现精确控制单分子释放的关键技术之一。
短脉冲光源
短脉冲光源指的是能够产生极短时间持续的光脉冲的光源,其持续时间通常在皮秒(10^-12秒)到飞秒(10^-15秒)范围内。这种短暂而强烈的光照能够精确地激活目标光敏蛋白,而不对细胞造成热损伤或其他不利影响。
激活机制
当短脉冲光照射到光敏蛋白上时,光能被吸收,引发光敏蛋白的构象变化。这一变化触发了蛋白质内部的一系列生物化学反应,最终导致与其结合的目标分子的释放。这一过程的精确性和快速性是通过控制光脉冲的持续时间、强度和波长来实现的。
光脉冲参数的调控
持续时间:短脉冲的持续时间直接影响光敏蛋白的激活效率,过短可能无法有效激活,过长则可能引起非特异性激活或细胞损伤。
强度:光脉冲的强度需精确控制,确保足够的能量达到光敏蛋白,实现有效激活。
波长:选择适合光敏蛋白吸收特性的光脉冲波长是实现特异性激活的关键。
短脉冲光源在光遗传学中的应用,极大地拓宽了单分子研究的可能性。通过精细调控光脉冲参数,研究人员能够在空间和时间上精确控制单分子的行为,从而深入理解其在细胞生命活动中的作用。
高尔基体的特殊作用
在细胞生物学中,高尔基体是细胞内重要的器官之一,负责蛋白质的修饰、排序和运输。在光遗传学释放单分子的过程中,高尔基体发挥着不可或缺的作用,成为实现精确控制单分子释放的关键环节。
高尔基体的基本功能
高尔基体由一系列平行排列的膜囊组成,它不仅是细胞内蛋白质加工的车间,也是蛋白质分泌的中转站。在光遗传学应用中,研究人员利用高尔基体的这些天然功能,为单分子的定位和释放提供了理想的平台。
在光遗传学中的应用
通过将光敏蛋白和目标分子共同定位到高尔基体,可以实现对目标分子的严格控制。当受到特定波长光照的激活后,光敏蛋白引发的结构变化能够触发目标分子从高尔基体释放到细胞内其他位置,或是分泌到细胞外。这一过程的精确度极高,几乎不受其他细胞内过程的干扰。
特殊作用的机制
定位精确性:高尔基体的特殊结构为光敏蛋白和目标分子提供了独特的微环境,有助于提高定位的精确性。
释放控制:光敏蛋白在高尔基体的激活可以通过细胞内信号传递路径精确控制,从而实现对目标分子释放时间和位置的精确控制。
功能多样性:高尔基体内的不同区域具有不同的生化环境,可以根据目标分子的特性选择最适合的区域进行定位和释放。
高尔基体在光遗传学释放单分子中的特殊作用,不仅为单分子研究提供了新的方法,也为细胞内物质运输和分泌机制的研究开辟了新的路径。随着对高尔基体功能的深入了解和光遗传学技术的不断发展,未来将有望在更多生物医学领域中发挥重要作用。
单分子成像技术的创新应用
单分子成像技术是一种能够观察和分析生物分子在单分子水平上行为的先进技术,为研究人员提供了研究细胞内复杂过程的新视角。该技术通过高灵敏度的光学设备和精细的实验方法,捕捉到单个分子的动态变化,揭示了许多传统宏观实验无法观察到的生物现象。
光学系统的关键组件
高性能显微镜:具有高分辨率和高信噪比的显微镜是实现单分子成像的基础设备,能够精确捕捉到单个分子的图像。
激光光源:用于提供稳定且具有特定波长的光照,激发标记在目标分子上的荧光标签。
高灵敏度探测器:如雪崩光电二极管(APD)或电子放大CCD相机,用于检测极低强度的荧光信号。
荧光标记的作用
在单分子成像技术中,荧光标记的选择至关重要。研究人员通常将荧光分子或荧光蛋白质标记到研究的目标分子上。当这些标记分子被激光激发后,会发出荧光,从而使目标分子在显微镜下可见。
成像技术的类型
荧光相关光谱(FCS):通过分析荧光强度随时间变化的关联函数,了解分子的扩散行为和浓度。
光学镊子:利用激光束捕获和操纵微小物体,用于研究单个分子的力学性质。
单分子荧光共振能量转移(smFRET):通过测量两个荧光分子间能量转移的效率,研究分子间的距离和相互作用。
数据分析与解释
单分子成像产生的数据量庞大且复杂,需要运用高级的图像处理软件和统计方法进行分析。通过这些分析,研究人员能够从单个分子的行为中提取出有关分子动态、相互作用和功能的重要信息。
光遗传学方法在单分子成像中的应用
光遗传学方法在单分子成像领域的应用,标志着生物医学研究进入了一个崭新的时代。通过精确控制光敏蛋白的活性,研究人员能够在单分子水平上观察和操纵生物分子的行为,从而深入理解细胞内复杂的生命过程。
光遗传学与单分子成像的结合
目标分子的精确操控:通过将光敏蛋白与特定的目标分子相结合,光遗传学技术能够实现对这些分子在细胞内位置和时间的精确控制。
高时空分辨率的观察:利用短脉冲光源激活光敏蛋白,研究人员可以在极短的时间尺度内观察分子的动态变化,提供高于传统显微镜技术的时空分辨率。
应用
单分子追踪:通过光遗传学技术,研究人员能够标记并追踪单个蛋白质或RNA分子在细胞内的移动路径,揭示其在细胞生命活动中的作用。
细胞信号传递研究:通过控制特定信号分子的释放,光遗传学方法可以用于研究细胞内的信号传递过程,如神经递质的释放和受体的激活。
细胞间相互作用:利用光遗传学操纵单个分子的行为,研究人员可以研究细胞间的相互作用,如免疫细胞识别和肿瘤细胞侵袭的机制。
实验中一般会遇到的挑战和解决方案
单分子成像技术在光遗传学中的应用虽然为生物学研究提供了前所未有的细致视角,但在实验过程中也面临了不少挑战。
挑战一:荧光标记的稳定性
在单分子成像实验中,荧光标记的稳定性是一个常见的问题。荧光分子可能会因光照而光解或猝灭,导致信号的丢失。
解决方案:
-使用光稳定性更好的荧光分子或荧光蛋白。
-优化光照条件,如降低激光强度、缩短照射时间。
-应用荧光恢复技术,如光漂白后的荧光恢复。
挑战二:背景噪音的干扰
单分子成像需要极高的信噪比,而细胞内杂质和其他荧光物质的存在常常造成背景噪音,影响观察精度。
解决方案:
-提高显微镜的空间分辨率,采用超分辨显微技术。
-使用更为特异的荧光标记,减少非特异性结合。
-应用先进的图像处理软件,通过算法减少背景噪音。
挑战三:样本制备的困难
要保持单个分子在自然状态下的活性和功能,同时使其能够被显微镜准确捕捉,是一项极具挑战的任务。
解决方案:
-优化样本制备流程,减少对分子活性的影响。
-开发新型的生物相容性载体,以更好地支持和保护样本。
-利用活细胞成像技术,减少样本制备对细胞状态的干扰。
挑战四:数据量巨大的处理与分析
单分子成像技术产生的数据量庞大,且数据的处理和分析十分复杂,给研究者带来了巨大的挑战。
解决方案:
-开发更为强大和高效的数据处理软件,提高数据处理的自动化和智能化水平。
-采用云计算和大数据技术,提高数据处理和存储的能力。
-引入机器学习和人工智能技术,提升数据分析的准确性和效率。
光遗传学方法在细胞功能重建中的应用
BK和LRRC8离子通道的重建
在细胞生理学中,BK和LRRC8离子通道扮演着至关重要的角色,它们参与调节细胞的电位平衡、体积控制以及信号传递等多个重要生理过程。通过光遗传学技术,研究人员现在能够在分子层面上重建这些关键的离子通道,从而为疾病治疗和生命科学研究开辟了新的道路。
BK离子通道的重要性
电生理功能:BK离子通道是一种大导电的钾通道,能够响应细胞内钙离子浓度的变化及膜电位的变化,从而调节神经元的兴奋性和肌肉细胞的收缩。
疾病关联性:BK通道的异常与多种疾病如高血压、哮喘和肌肉疾病等有密切联系。
LRRC8离子通道的作用
细胞体积调节:LRRC8通道是一种体积调节阴离子通道(VRAC),在细胞遇到渗透压变化时开放,参与细胞体积的调节。
参与细胞信号传递:LRRC8通道还与细胞内信号传递相关,包括细胞凋亡和细胞增殖等过程。
光遗传学技术在离子通道重建中的应用
基因编码的光敏蛋白:研究人员利用基因编辑技术,将光敏蛋白与BK或LRRC8离子通道蛋白融合,通过光照控制其活性,实现离子通道的开关。
精确的时空控制:通过调节光照的强度、持续时间和作用位置,光遗传学技术能够在极其精确的水平上模拟离子通道的自然调控机制。
功能重建与验证:重建后的离子通道能够在体外细胞模型中进行功能性验证,甚至在特定条件下应用于体内模型,为疾病治疗提供新策略。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


